-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ等(学生向け) TOEIC対策プログラム 博士人材のための就職支援(学生向け) 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会(企業向け) 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ等(企業向け) 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
がん細胞の生存・転移に重要なタンパク質を狙い撃ちする化合物を開発 -難治性がんに対する新しい治療薬の創出に期待-
2017.05.08研究成果Life & Health
九州大学生体防御医学研究所の福井宣規主幹教授、宇留野武人准教授、大学院医学系学府博士課程4年生の田尻裕匡らの研究グループは、東京大学大学院薬学系研究科の金井求教授、理化学研究所横山茂之上席研究員の研究グループと共同で、がん遺伝子Rasを介したがんの悪性化に、DOCK1というタンパク質が重要な役割を演じていることを発見し、その選択的阻害剤「TBOPP」を世界に先駆けて開発することで、DOCK1阻害によりがんの増殖および転移を抑制できることを実証しました。
がんは我が国の死因の第一位で、年間30万人以上の命を奪っており、重大な社会問題となっています。なかでもRas遺伝子の異常(変異)は、膵臓がんや大腸がんをはじめ多くのがんで認められ、がん全体の3分の1に及ぶにもかかわらず、いまだに有効な治療薬が無く、その対策は急務となっています。本研究グループは、変異Rasによるがんの生存および浸潤には、Racという分子の活性化が必要であることに着目し、その制御因子であるDOCK1の機能を解析しました。その結果、DOCK1を発現できないように遺伝子操作したがん細胞では、低栄養条件下での生存性および浸潤能が著しく低下することを見いだしました。そこで、20万を超える化合物ライブラリーをスクリーニングし、ヒット化合物の構造最適化を行い、DOCK1の選択的阻害剤(TBOPPと命名)の開発に成功しました。TBOPPをマウスに投与することで、変異Rasを有するがん細胞の増殖および転移が抑制できます。以上より、TBOPPは変異Rasを有するがんを治療するための新たな創薬リードになることが期待されます。
本研究成果は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業インキュベートタイプ(LEAP)および次世代がん研究シーズ戦略的育成プログラム(P-DIRECT)の成果で、2017年5月2日(火)正午(米国東部夏時間)に米国科学雑誌「Cell Reports」に掲載されました。
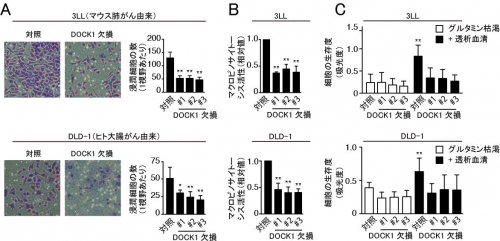
図1.Rasに変異を持つがん細胞の浸潤、マクロピノサイトーシス、および低栄養条件下での生存は、DOCK1の遺伝子欠損によって抑制される。
A: DOCK1欠損がん細胞では、対照となる細胞に比べて、浸潤能が抑制されている。
B: DOCK1欠損がん細胞では、対照となる細胞に比べて、マクロピノサイトーシスが抑制されている。
C: DOCK1欠損がん細胞では、対照となる細胞に比べて、低栄養条件下での生存性が低下する。
上段:3LL(マウス肺がん由来細胞)、下段:DLD-1(ヒトの大腸がん由来細胞)、#はクローン番号を示す
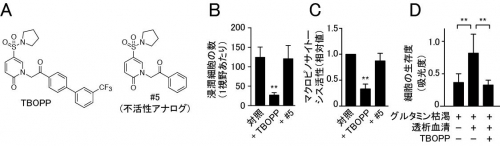
図2.DOCK1選択的阻害剤TBOPPは、変異Rasを有するがん細胞の浸潤、マクロピノサイトーシス、生存を抑制する。
A: TBOPPとDOCK1阻害活性のないアナログ(#5)の構造。
B: TBOPPは、マウス肺がん細胞株3LLの浸潤を抑制する。
C: TBOPPは、3LL細胞のマクロピノサイトーシスを抑制する。
D: TBOPPは、3LL細胞のグルタミン欠乏条件下での生存を抑制する。
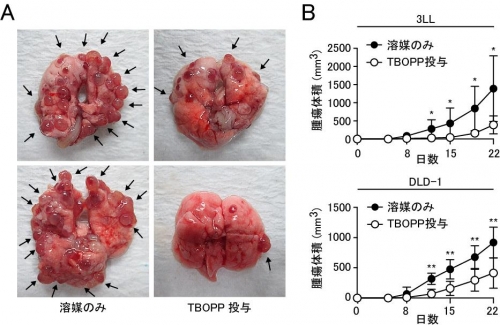
図3 DOCK1阻害剤の投与によって、がんの転移および増殖が抑制される。
A: 高転移性のマウス肺がん細胞株ex-3LLの肺転移は、TBOPP投与によって抑制される。
B: マウス肺がん細胞株3LL(上段)とヒト大腸がん細胞株DLD-1(下段)の増殖は、TBOPP投与によって抑制される。
研究者からひとこと
DOCK1阻害剤を開発し、がん治療に貢献したいという私達の夢が、一歩実現に近づきました。より効果的で、安全な新しい抗がん剤の創出を目指して、今後さらに研究を進めて参ります。
- 本研究についての詳細は こちら









































