Research Results 研究成果
食欲を抑え、熱産生を高めて末梢組織の糖利用を促進する神経細胞を発見 -インスリンの働きを高める脳の働きを解明し、肥満・糖尿病の予防と治療に期待-
2017.07.04研究成果Life & Health
骨格筋など末梢組織での糖の利用は、膵臓から分泌されるホルモン・インスリンによって促進されます。しかし、近年の研究により、脳、特に視床下部と呼ばれる脳領域の神経細胞が、単独或いはインスリンと協同して、末梢組織の糖の利用を促進することが明らかとなってきました。しかし、どの神経細胞が末梢組織の糖利用を促進するかは不明でした。今回、自然科学研究機構生理学研究所の箕越靖彦教授、吉村由美子教授、小林憲太准教授、星薬科大学の塩田清二特任教授、九州大学大学院医学研究院および東京医科歯科大学大学院医歯学総合研究科の小川佳宏教授らの共同研究グループは、視床下部腹内側核の神経細胞において、SF1/Ad4BPニューロンを直接化学的に刺激すると、食欲を抑え、熱産生を高めると共に、骨格筋などの末梢組織においてインスリンの働きを高めて糖の利用を促進することを、マウスを用いて明らかにしました。肥満の原因となる白色脂肪細胞への糖の取込は促進しませんでした。
本研究結果は、2017年7月3日(月)、アメリカ糖尿病学会学会誌diabetesのオンライン版に掲載されました。
<概要>
私達の体には、脂肪細胞で産生されて血中に分泌される、レプチンと呼ばれるホルモンがあります。レプチンは、主に視床下部の神経細胞(ニューロン)に作用を及ぼして、食欲を抑え、熱産生を高めます。箕越教授の研究グループは、これらの作用に加えて、レプチンが視床下部、中でも視床下部腹内側核の神経細胞に直接働き、骨格筋などの末梢組織においてインスリンの働きを高め、糖の利用を促進することを報告してきました。事実、レプチンの産生場所である脂肪細胞が消失する病気、「脂肪萎縮症」は、血中レプチン濃度が低下し、重症の糖尿病を発症します。この病気では、膵臓からインスリンはたくさん分泌されるのですが、骨格筋や肝臓においてインスリンの働きが低下するため、インスリンによる治療もほとんど効果がありません。ところが、レプチンを投与すると、この病気の糖尿病が著しく改善することが明らかとなり、現在では、同病気の治療薬として世界中で利用されようになりました。このように、どの神経細胞が、骨格筋など末梢組織でのインスリンの働きを高めて、糖の利用を促進するかを解明することは、新しい糖尿病治療の開発にもつながる可能性があります。箕越教授の研究グループは、レプチンが視床下部腹内側核ニューロンに作用することで、その効果を発揮すると考えてきました。しかし、視床下部腹内側核ニューロンには、様々な機能を持つ神経細胞が存在します。例えば、糖尿病のように、血糖を逆に上昇させる神経細胞も存在します。それ故、血糖を上昇させず、糖利用を促進する視床下部腹内側核ニューロンを明らかにすることが必要です。本研究グループは、視床下部腹内側核ニューロンの中で、末梢組織の代謝に調節作用を及ぼすと考えられるSF1/Ad4BPニューロン(以下、SF1ニューロン)に注目し、その機能を調べました。
研究グループは、SF1/Ad4BPニューロンの神経活動を選択的に高めるために、今回、DREADD法(Designer Receptors Exclusively Activated by Designer Drug)という、特定の神経細胞の神経活動を増加したり、抑制することができる方法を使い、実験を行いました。この方法によってマウスのSF1ニューロンを選択的に活性化すると、摂食量が低下して、熱産生が高まると共に、全身の糖利用が促進しました。そこで、どの組織に糖の取込が高まるかを調べたところ、エネルギー消費器官である骨格筋、心臓、褐色脂肪組織において選択的に糖の取込が高まることがわかりました。脂肪を貯蔵する白色脂肪組織では、糖の取込は全く変化しませんでした。また、インスリンを投与すると、SF1ニューロンを活性化したマウスは、活性化しないマウスに比べて、糖の取込が骨格筋、心臓、褐色脂肪細胞において増加し、結果として、全身で見ても糖利用も顕著に促進しました。
以上の実験結果から、SF1ニューロンを活性化すると、レプチンをマウスに作用させた時と同様に、摂食量や熱産生に作用を及ぼして抗肥満効果を引き起こし、まるで運動のように、糖取込の最大組織である骨格筋においてインスリンの働きを高めて、糖の取込を促進することが分かりました。骨格筋細胞などの細胞膜にはインスリン受容体蛋白質があります。インスリンは、インスリン受容体蛋白質に結合すると、情報を細胞内に伝え、Aktなどいくつかの細胞内タンパク質を活性化して、糖の取込を促進します。本研究により、SF1ニューロンを活性化すると、インスリン受容体とAktが共に活性化することを見出しました。この実験結果から、SF1ニューロンを活性化すると、骨格筋によってインスリンの働きが高まり、その結果、糖の取込が亢進したと考えられます。SF1ニューロンがどのようにして骨格筋でのインスリン作用を増強するかは、まだ明確には分かっていませんが、別の研究から、交感神経を介することが示唆されます。
以上、本研究によって、視床下部腹内側核に存在するSF1ニューロンをDREADD法によって活性化すると、摂食量が低下して熱産生が上昇すると共に、骨格筋など末梢組織においてインスリンの働きが高まり、糖の利用が増加することが分かりました。今回の発見は、肥満や糖尿病の病因解明、新しい治療法の確立に繋がることが期待されます。
本研究は、国立研究開発法人日本医療研究開発機構の革新的先端研究開発支援事業(AMED-CREST)「生体恒常性維持・変容・破綻機構のネットワーク的理解に基づく最適医療実現のための技術創出」研究開発領域における研究開発課題「細胞間相互作用と臓器代謝ネットワークの破綻による組織線維化の制御機構の解明と医学応用」(研究開発代表者:小川佳宏)の一環で行われました。また、日本学術振興会 科学研究費補助金基盤研究B(代表研究者:箕越靖彦教授)の支援も受けました。
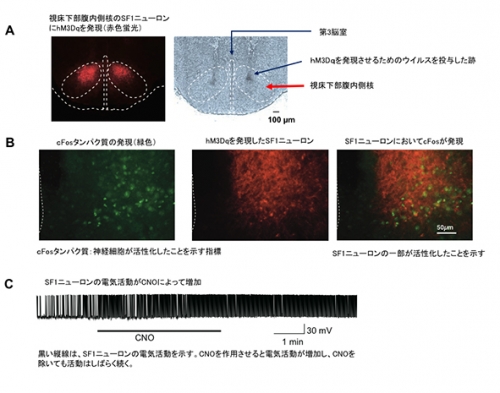
マウスSF1ニューロンの神経活動がDREADD法により増加
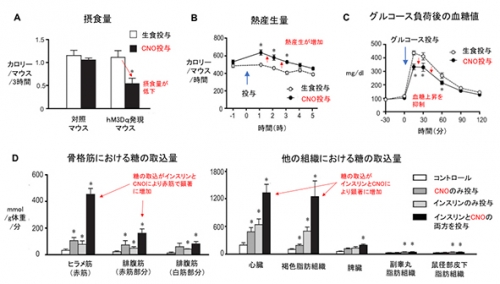
SF1ニューロンの神経活動を高めると、摂食量が低下、熱産生が増加すると共に、インスリンによる糖利用が促進する
- 本研究についての詳細は こちら
論文情報
Activation of SF1 Neurons in the Ventromedial Hypothalamus by DREADD Technology Increases Insulin Sensitivity in Peripheral Tissues ,Diabetes,10.2337/db16-1344









































