-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ等(学生向け) TOEIC対策プログラム 博士人材のための就職支援(学生向け) 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会(企業向け) 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ等(企業向け) 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
光親和性標識法の新たな分子ツール-疎水性が低くコンパクトな光反応性基-
2018.02.22研究成果Life & HealthPhysics & Chemistry
理化学研究所(理研)袖岡有機合成化学研究室の平井剛客員研究員(九州大学大学院薬学研究院教授)、太田英介特別研究員(研究当時)、袖岡幹子主任研究員(環境資源科学研究センター グループディレクター)らの共同研究グループは、薬剤(生物活性分子)の結合タンパク質同定手法の一つである「光親和性標識法」に利用可能な新たな分子ツールとして、2-チエニル置換型α-ケトアミド構造を開発しました。
光親和性標識法は、生物活性分子の結合タンパク質同定に用いられるケミカルバイオロジー研究には欠かせない手法の一つです。この手法では、光によって結合タンパク質と共有結合を形成する「光反応性基」を用います。従来の光反応性基は十分な反応性を発揮させるために、疎水性で嵩(かさ)高い構造が必要でした。そのため、真の結合タンパク質以外のタンパク質とも非特異的に相互作用し、共有結合を形成するという欠点がありました。しかし、この欠点を克服した新たな光反応性基の開発はほとんど行われてきませんでした。
今回、共同研究グループは、α-ケトアミド構造が光反応性基として機能すると考え、α-ケトアミド構造を生物活性分子としてマンノース構造に連結した分子ツールを作製し、タンパク質のコンカナバリンAとの光親和性標識実験を行いました。その結果、チエニル基を持つα-ケトアミド(2-チエニル置換型α-ケトアミド構造)が良好な反応性を示し、光反応性基として十分機能することを見いだしました。この新しい光反応性基は、従来のものよりも疎水性が低くコンパクトで、非特異的な結合が著しく抑制できることが分かりました。
本成果は生理活性天然物や薬剤だけでなく、ペプチド、タンパク質、糖鎖、核酸、脂質など幅広い分子群と結合タンパク質の相互作用の解析に利用可能な分子ツールとして有望と考えられます。また、チエニル基の効果をさらに研究することで、今後、より機能性の高い光反応性基の開発につながると期待できます。
本研究は、米国の科学雑誌『ACS Chemical Biology』オンライン版(2月19日付け)に掲載されました。
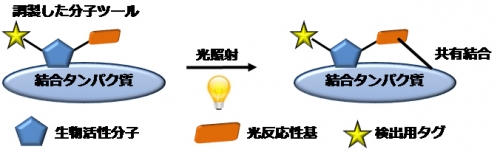
図1 光親和性標識法の概略図
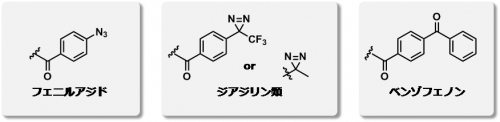
図2 代表的な光反応性基
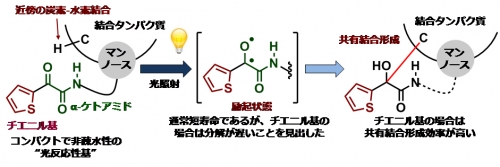
図3 新たに開発した光反応性基:チエニル基置換型α-ケトアミド
- 本研究についての詳細は こちら
論文情報
Thienyl-Substituted α-Ketoamide: A Less Hydrophobic Reactive Group for Photo-Affinity Labeling ,ACS Chemical Biology,10.1021/acschembio.7b00988









































