-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ等(学生向け) TOEIC対策プログラム 博士人材のための就職支援(学生向け) 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会(企業向け) 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ等(企業向け) 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
世界初!ヘテロクロマチンによる染色体異常の抑制を発見 ~ゲノム編集を伴わない遺伝子治療につながる成果~
2019.01.15研究成果Life & HealthPhysics & Chemistry
【研究成果のポイント】
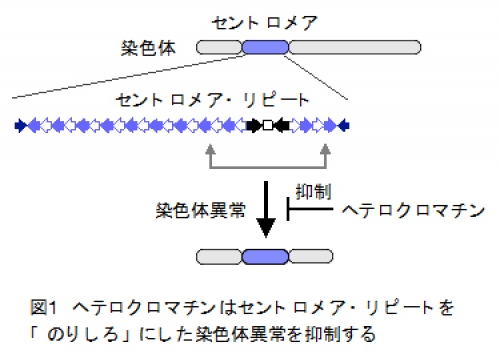
◆ 染色体のヘテロクロマチン※1がセントロメア領域※2のDNAの反復配列※3を「のりしろ」にした染色体異常※4を抑制することを世界で初めて発見
◆ ヒトと類似したクロマチン構造を持つ分裂酵母※5を用いて、ヘテロクロマチンによる転写※6制御が染色体異常を抑制することを明らかに
◆ ゲノム編集(変異)を伴わない、クロマチン制御による遺伝子治療への応用に期待
大阪大学大学院理学研究科の中川拓郎准教授、沖田暁子大学院生らの研究グループは、北海道大学の村上洋太教授、東京工業大学の木村宏教授、九州大学の高橋達郎准教授との共同研究でヘテロクロマチンがセントロメア領域のDNA反復配列(セントロメア・リピート)を「のりしろ」にした染色体異常を抑制することを世界で初めて明らかにしました(図1)。
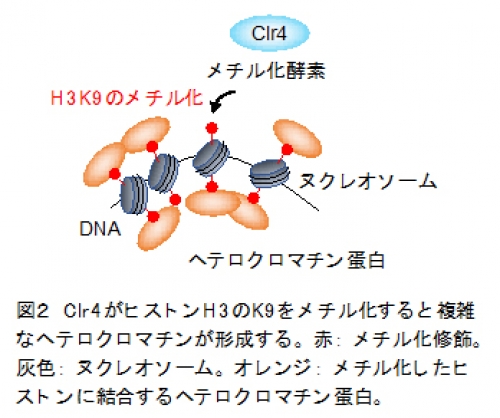
生命の遺伝情報を担う染色体は、DNAがヒストン※7というタンパク質に巻き付いたヌクレオソーム※8(図2、灰色)を基本単位とするクロマチン構造を形成します。染色体のセントロメア領域には、DNAの反復配列(セントロメア・リピート)が存在し、凝縮したヘテロクロマチン構造が形成されます。DNA複製の進行停止などによりDNA損傷が自然発生的に起きた際、反復配列を「のりしろ」にして転座などの染色体異常が起こることがあります。こうした染色体異常がセントロメア周辺で起こるロバートソン転座※9は、ヒトで最もよく見られる染色体異常ですが、どのように制御されているのか明らかとなっていませんでした。
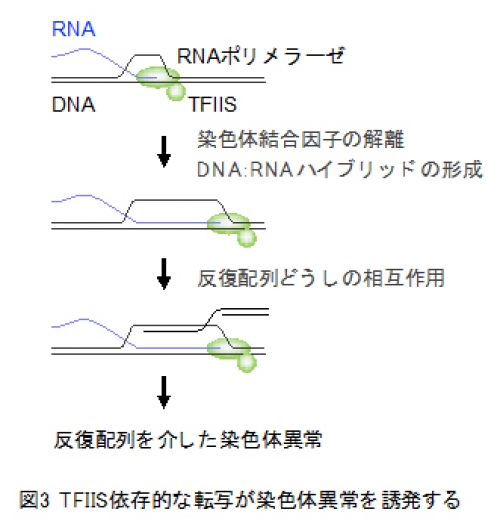
本研究では、分裂酵母を用いて染色体の安定性におけるヘテロクロマチンの役割を調べました。その結果、ヘテロクロマチンの基盤であるヒストンH3の9番目のリシン残基(H3K9)のメチル化修飾(図2)が、セントロメア・リピートを「のりしろ」にした染色体異常の抑制に重要であることを発見しました。通常、ヘテロクロマチンを形成する DNA領域では、DNAを鋳型にRNAを合成する転写が不活化されています。ヘテロクロマチンによる染色体異常の抑制メカニズムを明らかにするため、ヘテロクロマチンが形成できない変異株を詳細に調べたところ、転写伸長を促進する転写因子TFIIS※10が染色体異常を誘発することが明らかになりました(図3)。
本研究により発見した「ヘテロクロマチンの転写制御を介した染色体異常の抑制機構」は、ゲノムの半分以上を反復配列が占めるヒトなどの高等真核生物では、より重要な役割を担っていると考えられます。
本研究成果により、DNA変異を加えることなくクロマチン構造のみを操作することで、人為的に染色体の安定性を高められることが期待されます。
本研究成果、はSpringer Nature社の科学誌「Communications Biology」(オンライン)に、2019年1月11日(金)19時(日本時間)に公開されました。
- 本研究についての詳細は こちら
論文情報
Heterochromatin suppresses gross chromosomal rearrangements at centromeres by repressing Tfs1/TFIIS-dependent transcription ,Communications Biology,10.1038/s42003-018-0251-z









































