-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ等(学生向け) TOEIC対策プログラム 博士人材のための就職支援(学生向け) 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会(企業向け) 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ等(企業向け) 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
がんの悪性化における窒素代謝の変化を解明 -難治性がんの新たな治療標的PPATを発見-
2020.03.18研究成果Life & Health
九州大学生体防御医学研究所の中山 敬一 主幹教授、医学系学府博士課程4年の小玉 学 大学院生と新潟大学大学院医歯学総合研究科の松本 雅記 教授らの研究グループは、次世代プロテオミクス技術であるiMPAQTシステムを駆使したがん代謝解析から、悪性のがんではグルタミン由来の窒素をDNAの合成に利用するための代謝系が亢進していること(窒素シフト)を明らかにしました。
炭素と窒素は生体の主要な構成要素であり、それぞれ主にグルコースとグルタミンという二大栄養素から供給されます。がん細胞では炭素源であるグルコースを嫌気的に代謝する「ワールブルグ効果」が亢進していること(炭素シフト)が約100年前から知られていました。一方で、がん細胞は盛んに増殖しているので、窒素を含むDNAを多量に作る必要がありますが、今まではがん細胞がどのようにグルタミンからDNAに窒素を効率よく配分しているのかは不明でした。
そこで本研究グループは、独自に開発したiMPAQTシステムを用いて、がん細胞の悪性化に伴う代謝酵素の発現変化を追跡しました。その結果、悪性化したがん細胞では、グルタミンの窒素をDNAの前駆体に転移するPPATという代謝酵素が高発現しており、それによって生じるグルタミンからの窒素代謝シフトが、がんの悪性化の過程に必須であることを明らかにしました。更に公共データベースに登録されている11,000人のがん患者のメタアナリシスから、PPATが約1200種のヒト全代謝酵素の中で最もがん患者の死亡リスクを高める因子であり、特に小細胞肺がんをはじめとした難治性がんを治療する上で有望な標的になることを世界に先駆けて発見しました。これらの成果は、現在治療が困難とされている小細胞肺がんをはじめとした難治性がんに対して、PPATの阻害薬(現在開発中)が効果的な治療法となる可能性を示しています。本研究成果は、2020年3月17日(火)(米国東部時間)に英国科学雑誌「Nature Communications」で公開されました。
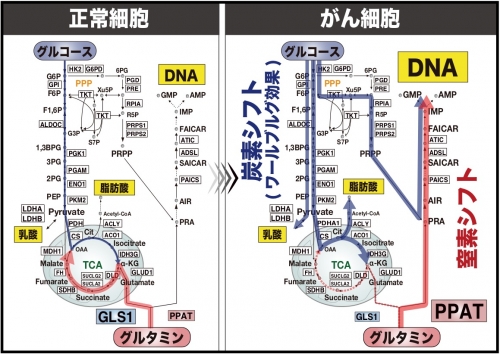
参考図 がん悪性化に必須のグルタミン窒素代謝シフト
研究者からひとこと
悪性化したがん細胞はPPATを発現上昇させることでグルタミンの窒素からDNAを効率的に合成します。このPPATの反応を阻害することで、がん細胞の増殖を効果的に抑制できることから、今まで治療困難であった難治性がんの新規治療法となる可能性が示唆されます。
- 本研究についての詳細は こちら
論文情報
A shift in glutamine nitrogen metabolism contributes to the malignant progression of cancer ,Nature Communications,https://doi.org/10.1038/s41467-020-15136-9









































