-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ TOEIC対策プログラム 博士人材のための就職支援 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
立体的に大きな非天然α-アミノ酸の新たな合成法を開発
非天然α-アミノ酸を持つ中分子ペプチド創薬への応用に期待 2020.05.01研究成果Life & Health
α-アミノ酸は私たちの体をつくるたんぱく質の構成成分として、生命活動を維持するための重要な役割を担っています。また最近では、創薬分野において低分子と抗体の特徴を有した中分子ペプチド、中でも天然には存在しない非天然α—アミノ酸を有する中分子ペプチドが革新的な次世代型医薬品として期待されています。そのため非天然α—アミノ酸の合成法は古くより盛んに研究が行われてきました。しかし立体的に大きな非天然α—アミノ酸、特に連続して立体的に大きな部位をもつ非天然α—アミノ酸の合成はこれまで非常に困難で、その機能を調べるための一般性の高い合成法の開発が強く望まれていました。このような背景のもと、九州大学大学院薬学府修士課程2年の松本洋平大学院生(研究当時)、薬学研究院の矢崎亮助教、大嶋孝志教授らと山口大学大学院創成科学研究科応用化学分野の西形孝司教授らの研究グループは、立体的に大きな非天然α—アミノ酸を効率的に合成する手法の開発に世界に先駆けて成功しました。
非天然α—アミノ酸の原料としてO’Donnell教授らによって40年以上前に開発されたアミノ酸Schiff塩基が広く用いられてきましたが、これまでは立体障害に弱いイオン型の反応機構に限定されていました。今回研究グループでは、大きな立体障害を克服するために反応性の高いラジカル型の反応機構に着目し、銅触媒を用いることでアミノ酸Schiff塩基を世界で初めてラジカル型機構で反応させることに成功しました。今回の合成手法を用いることで、様々な種類の立体的に大きな非天然α—アミノ酸合成が可能で、光学活性なα—アミノ酸への展開にも成功しました。本成果により、今後立体的に大きな非天然α—アミノ酸の機能評価や、中分子ペプチド医薬品などの様々な機能性分子創製への応用が期待されます。以上の研究成果は、アメリカ化学会が出版する国際誌「Journal of the American Chemical Society」に2020年4月22日(水)(アメリカ時間)にオンライン版に掲載されました。
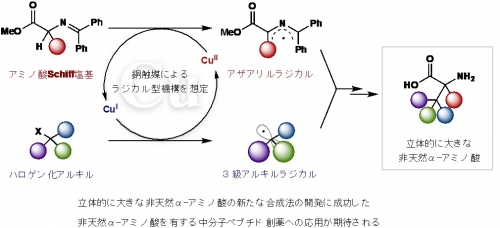
(参考図)
アミノ酸Schiff塩基の銅触媒によるラジカル機構による立体的に大きな非天然α—アミノ酸合成法の概要。本反応光学活性α—アミノ酸を含め様々な非天然α—アミノ酸の合成に成功した。
研究者からひとこと
立体的に大きな非天然α—アミノ酸合成法、またラジカル機構によるアミノ酸Schiff塩基の活性化法の基盤技術として、様々な研究分野での応用が期待されます。今後は中分子ペプチド創薬研究へと展開し、非天然α—アミノ酸の可能性を広げて行きたいと考えております。
- 本研究についての詳細は こちら
論文情報
Amino Acid Schiff Base Bearing Benzophenone Imine As a Platform for Highly Congested Unnatural α-Amino Acid Synthesis ,Journal of the American Chemical Society,10.1021/jacs.0c02707









































