-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ等(学生向け) TOEIC対策プログラム 博士人材のための就職支援(学生向け) 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会(企業向け) 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ等(企業向け) 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
脂肪細胞の表面にある受容体シグナルが脂肪分解を促すことを発見!
2021.02.10研究成果Life & HealthPhysics & Chemistry
GPRC6AはGタンパク質共役型受容体※の一種です。九州大学大学院歯学研究院OBT研究センターの向井悟学術研究員(研究当時、現東亜大学医療学部准教授)、溝上顕子准教授、福岡歯科大学口腔医学研究センターの平田雅人客員教授らの研究グループは、脂肪細胞におけるGPRC6Aシグナル不全が脂肪の分解を抑制し、食餌誘発性の肥満とそれに起因する代謝異常を引き起こすことを明らかにしました。
GPRC6Aは、骨ホルモンであるオステオカルシン、オルニチンといったアミノ酸、テストステロン、細胞外Ca2+などの多様な分子に応答します。GPRC6Aを持たないマウスは、メタボリックシンドロームが進行したり、骨量が減少したりと様々な異常を示すことが既に報告されていましたが、その詳細な役割は不明でした。研究グループはこれまでに、特に脂肪細胞のGPRC6Aがオステオカルシンにより活性化し、脂肪細胞を縮小させることを明らかにしています。そこで、脂肪細胞におけるGPRC6Aシグナルが重要ではないかと考え、脂肪特異的にGPRC6Aを持たないマウス(adG6AKO)を作成し、GPRC6Aを介したシグナル経路が脂肪蓄積を制御するメカニズムを解析しました。
adG6AKOマウスを高栄養食で飼育すると、GPRC6Aを持つマウスと摂食量はほぼ同じであるにも関わらず体重増加が著しいことがわかりました。また、adG6AKOマウスの脂肪細胞は著しく肥大しており、肝臓への脂肪蓄積も顕著でした。脂肪細胞における脂肪酸取り込み、中性脂肪合成、脂肪分解の各ステップに関わる分子群の発現を比較したところ、adG6AKOマウスの脂肪組織では脂肪を分解する酵素群が著しく減少しており、脂肪分解が抑制されていることがわかりました。その結果adG6AKOマウスでは肥満、高血糖、耐糖能異常などのメタボリックシンドローム様を呈することがわかりました。
さらに、GPRC6Aは多様な分子に応答しますが、本研究では脂肪分解酵素の発現を上昇させるにはオステオカルシンとオルニチンが最も有効であったことから、脂肪細胞をオステオカルシンやオルニチンで刺激したところ、脂肪分解酵素群の発現は増加しました。つまり、adG6AKOマウスの肥満は、オステオカルシンやオルニチンによる恒常的なGPRC6Aシグナルがなくなったことによって脂肪分解酵素が減少し、脂肪分解が抑制されたことに起因することを示します。脂肪細胞におけるGPRC6Aシグナルの恒常的な活性化が脂肪の分解を促進し、全身の代謝調節に重要な役割を果たしていることが明らかになりました。
本研究成果は、2021年1月9日(米国時間)に米国科学雑誌「Journal of Biological Chemistry」で公開されました。
【用語の解説】
※ Gタンパク質共役型受容体
細胞膜上に存在する受容体の一種。神経伝達物質やホルモンなどの様々なシグナルを受容して構造を変化させ、細胞内のGタンパク質を介して細胞内に情報を伝達する。細胞膜を 7 回貫通する特徴的な構造をもつことから、別名 7 回膜貫通型受容体ともよばれる。
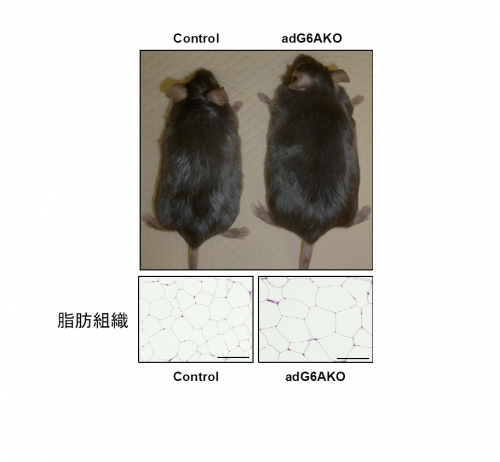
左が通常のマウス、右がadG6AKOマウス。
adG6AKOマウスの脂肪組織では、脂肪細胞が著しく肥大している。
研究者からひとこと
脂肪組織におけるオステオカルシンやオルニチンによる恒常的なGPRC6Aシグナルが肥満を抑制することが今回明らかになりました。この成果が肥満治療法開発につながればと思います。
- 本研究についての詳細は こちら
論文情報
Adipocyte-specific GPRC6A ablation promotes diet-induced obesity by inhibiting lipolysis ,Journal of Biological Chemistry,10.1016/j.jbc.2021.100274









































