-
カテゴリ別
-
場所
-
最新のお知らせ 年間スケジュール(就職対策講座等) OB・OG情報 システムの利用方法 学内合同企業説明会(「九州大学生のための業界・企業研究」) 学内企業研究セミナー / 個別企業説明会 公務員・教員等採用情報 就職相談 就職情報室 キャリア教育 低年次学年向け情報 インターンシップ等(学生向け) TOEIC対策プログラム 博士人材のための就職支援(学生向け) 外国人留学生のための就職支援 未内定の学生及び既卒者(卒業後3年以内)の皆様へ 障害のある学生のための就職支援 部局独自の就職支援 東京・大阪・博多駅オフィスの利用 各種情報サイト 過去の就職状況 採用選考に関する指針 学内合同企業説明会 博士人材のための企業説明会(企業向け) 本学へのご訪問 求人情報ご提供 OB・OG名簿ご提供 インターンシップ等(企業向け) 外国人留学生の採用 採用選考に関する指針 就職担当 よくあるご質問
Research Results 研究成果
がん組織の高い温度に反応し、ナノ微粒子が特異的に集積する仕組みを開発 ~副作用のないがん治療へ期待~
2017.03.08研究成果Life & Health
JST 戦略的創造研究推進事業において、九州大学 大学院薬学研究院の唐澤 悟 准教授らは、がん組織の温度に応答して薬剤分子を集める仕組みを開発しました。
ドラッグデリバリーシステム(DDS)は体内の薬剤分布を量的、空間的、時間的に制御する薬剤運搬技術で、がん治療の1つとして研究が進んでいます。従来は、血管に生じる「隙間」を利用して、数十~百ナノメートルサイズのナノ微粒子中に薬剤を内包させ、がん病巣へ薬剤を集積させます。しかし、この方法では薬剤が正常な組織にも分布するため、副作用を発症するなどの問題がありました。そのため、がん組織のみを狙う高精度ながん集積法を持つDDS開発が望まれていました。
がん組織は、活動が活発なため正常な組織よりも温度が高いことが知られています。唐澤准教授らは、温度が変わると分子が集合して形やサイズが変化する「温度応答性ナノ微粒子」を研究し、がん組織に分子を集めて留まる方法を新たに開発しました。このナノ微粒子は、ヒトの体温よりも少し高温の温度域で自ら集合して大きなサイズになります。がんを持つマウスへ蛍光分子を取り付けたナノ微粒子を投与したところ、がん細胞の温度に応答してナノ微粒子ががん組織に集積する様子が蛍光イメージングで観察されました。
この方法を利用することで、従来のDDSが抱えていた、がん細胞以外への副作用を解決するだけではなく、低い投与量で負担が少ない、新たながん診断や治療に役立つことが期待されます。
本研究は、九州大学 大学院薬学研究院の荒木 健さん、臼井 一晃 助教、量子科学技術開発機構の青木 伊知男 博士、村山 周平 博士らと共同で行ったものです。
本研究成果は、2017年3月7日(米国東部時間)に米国科学誌「Nano Letters」のオンライン速報版で公開されました。
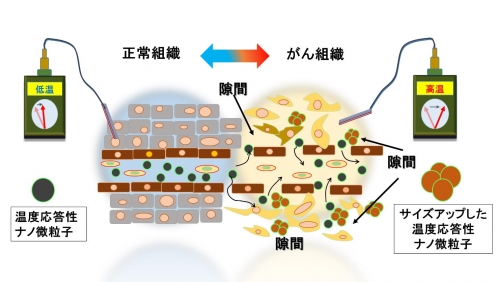
図1 正常組織とがん組織との形態と温度の違い
がん組織中には、血管内皮細胞の周辺に数十~数百ナノメートルの隙間や、がん細胞自身の周辺にも隙間が生じる。また、がん細胞は活発に活動するため正常組織よりも温度が高く、乳腺がんが2℃程度高温であると報告された例がある。本研究で開発した温度応答性ナノ微粒子(緑色の球)はがん組織の隙間に入り込みサイズアップし(茶色の球)、がん中に留まるように設計を行った。
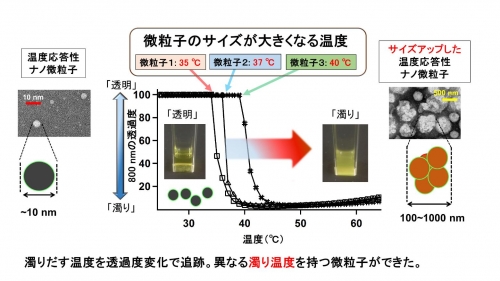
図2 微粒子が温度に反応してサイズアップする様子
微粒子を含む「透明」溶液を加温すると微粒子のサイズが大きくなり、「濁り」溶液に変化する。微粒子の透過型電子顕微鏡写真と微粒子が温度に反応してサイズアップする様子を透過度変化の温度依存性で示した。濁り始める温度が異なる3種類の微粒子を作り分けた。
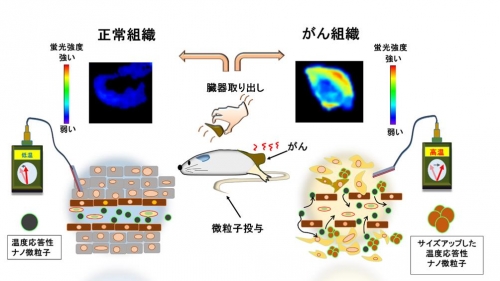
図3 担癌マウスへの微粒子投与実験
蛍光分子を取り付けた微粒子1は、35℃以上でサイズアップする。担癌マウスへ、この微粒子1を投与し、蛍光イメージングで組織を観察した結果、がん組織付近のみに強い蛍光が観測された。これにより、温度の高いがん組織へ特異的に微粒子が集積・サイズアップし、正常組織には集まらないことが確認された。
- 本研究についての詳細は こちら
論文情報
Self-Assembly Behavior of Emissive Urea Benzene Derivatives Enables Heat-Induced Accumulation in Tumor Tissue ,Nano Letters,10.1021 /acs.nanolett.6b05371









































